|
|
|
|
| 2章 いろいろな水 | 小林 映章 |
|
2.2 処理の異なる水
2.2.2 電解水
三洋電機の電解応用洗濯機は「水溶液」の電気分解を応用したものとして、画期的ですが、これとは別に「水」に電気分解を適用した、価値ある電解水というのが以前から知られています。ここでは、電解水、並びに水の電気分解を利用して製造したと云われているアルカリイオン水の2つについて考えてみます。
(1)電解水
H2O
しかし、水の電離はほんの僅かで、25℃における水素イオンと水酸化物イオンの濃度の積、すなわち、イオン積(〔H+〕×〔OH-〕)が1×10-14に過ぎず、生成したイオンの量はごく少量しかありません。したがって、水はそのままでは電気を通さないため、電気分解を行うことができません。そこで水の電気分解を行うには、適当な電解質を加えてイオンの数を増やしてやることが必要です。例えば、電解質として水酸化ナトリウム(NaOH)を水に添加した場合には、次のようにして水の電気分解が起こります。
水酸化ナトリウムは水中で大部分の分子がイオンに解離しています。
NaOH
アノード、カソードにおける反応は次のようになります(電子の出入りは省略しました)。 アノード(+極): 4OH- → 2H2O + O2
上式はよくみますと、水酸化ナトリウムの電解反応であって、水はその副作用として、結果的に次のように電気分解されたことになります。 2H2O → O2 + 2H2
つまり水の電気分解とは、溶存する電解質の電気分解であって、水は副次的に電気分解されているわけです。 【(1) 電気分解では、正電荷(電流)が溶液側から流入する電極を陰極(cathode)、正電荷が溶液側へ流出する電極を陽極(anode)と云います。電池(放電反応)では正電荷が溶液側から流入する電極を正極(cathode)、溶液側へ流出する電極を負極(anode)と云います。このように電解と電池で区別する呼び方は紛らわしいので、正電荷が溶液側から流入する電極(陰極、正極)をカソード、溶液側へ流出する電極(陽極、負極)をアノードと統一的に呼ぶことが推奨されています。
(電解水)
うすい食塩水を隔膜で仕切り、膜の両側に電極を挿入して電気分解を行ったとき、アノード側に強酸性電解水と称する水溶液ができます。殺菌力が強く残留性がないことから、驚異の水として病院や食品業界で話題になりました。
機能水研究所がこの水を分析した結果が発表されています。その結果は殺菌力のある主成分として次亜塩素酸(HClO)と分子状塩素(Cl2)が検出されています。これはアノード側に移動したCl-が電極で電子を放出してCl2となるとともに、水と反応して次亜塩素酸が生成したものです。次亜塩素酸はpH5付近で最も殺菌力が強く、この条件が揃ったものです。この例はいわゆる電気分解で機能的な水が作り出されたものといえます。
ただ一言付け加えるならば、次亜塩素酸の水溶液に希塩酸を加えてpH5前後に調節すれば、強酸性電解水と同じ水が得られます。こうすれば、高価な電解水製造器を必要としないことになります。 |
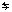 H+ + OH-
H+ + OH-